|
检测试剂盒再成“香饽饽”!海外疫情大爆发点燃需求信号? 时间:2020.03.30 17:54 新一周依然是由疫情的进展开启。 [size=+0]根据[size=+0]美国约翰斯·霍普金斯大学公布的实时疫情数据显示,截至北京时间3月30日上午8时22分,[size=+0]全球新冠肺炎累计确诊病例已升至72万[size=+0],达721584例;累计死亡数达33958例。 [size=+0]不得不说,这一数字多少有些触目惊心,全球疫情的爆发还在继续,虽然国内疫情的逐步受控,但整体的现状依旧无法忽视,而在这期间,基于疫情需要,尤其是[size=+0]在海外国家的海量需求之下,[size=+0]核酸[size=+0]检测[size=+0]试剂盒[size=+0]依旧是“千金难买”的可贵之物[size=+0]。 [size=+0]事实上,按[size=+0]中国疾控中心[size=+0]的标准来看,[size=+0]目[size=+0]前批准上市的新冠肺炎检测试剂主要包括两类,[size=+0]第[size=+0]一类是核酸检测试剂[size=+0],检测过程包括标本处理、核酸提取,进行PCR检测等多个步骤,平均检测时间需要2-3个小时[size=+0],[size=+0]具备[size=+0]特异性强[size=+0]、[size=+0]敏感度相对较高[size=+0]等特点,[size=+0]是目前防控疫情的主要[size=+0]检测手段[size=+0];[size=+0]第二[size=+0]类是抗体检测试剂[size=+0],[size=+0]包括胶体金法和磁微粒化学发光法[size=+0], [size=+0]截至3月27日,[size=+0]根据[size=+0]国家药监局官网显示,[size=+0]一[size=+0]共批准新冠病毒核酸检测试剂盒15个,抗体检测试剂盒8个。 [size=+0]基于上述,[size=+0]本着互帮互助的大国情怀,[size=+0]相对于一些[size=+0]低效率的试剂检测[size=+0],[size=+0]我国在技术不断进化之下而升级的核酸检测[size=+0]试剂盒[size=+0]便在满足国内需求的同时,也开启了其“出海之旅”,[size=+0]目前已有23个新冠肺炎检测试剂盒获批,且[size=+0]部分[size=+0]企业获得欧盟等认证,[size=+0]其[size=+0]出口[size=+0]之势较为迅猛[size=+0]。 [size=+0]然而,在出口的路途之上,由[size=+0]试剂盒[size=+0]所引发的“乌龙”也不少。 [size=+0]例如,[size=+0]菲律宾卫生部29日[size=+0]发表声明,对该部门一名官员在28日记者会上称“中国援菲试剂盒准确率仅40%”引发的误导性言论表示道歉, [size=+0]强调中国政府援菲试剂盒[size=+0]([size=+0]华大基因核酸检测试剂盒和圣湘核酸检测试剂盒[size=+0])[size=+0]质量与世界卫生组织提供的试剂盒相当[size=+0],[size=+0]并作出澄清[size=+0],[size=+0]称[size=+0]该官员所称的试剂盒不是由中国政府捐赠,而是由一家私人基金会拟捐赠的。  [size=+0]来源于:官方文件 [size=+0]与此同时,日前[size=+0]西班牙《国家报》发表题为“[size=+0]购买的来自中国的易瑞生物(Bioeasy)公司[size=+0]的新冠病毒快速检测试剂效果不佳”的文章[size=+0],[size=+0]指出其试剂的效果不如预期——原本检测结果符合率应该在80%以上,但实际上却仅有30%,但随后我国[size=+0]相关部门宣布, [size=+0]西班牙以4.32亿欧元向中国购买的医疗物资([size=+0]包括550万份核酸检测试剂盒[size=+0])里没有易瑞生物的产品,且该公司也并未获得国家药监局的官方销售许可[size=+0]。目前[size=+0]深圳市场监管部门已经对其启动了快速核查。 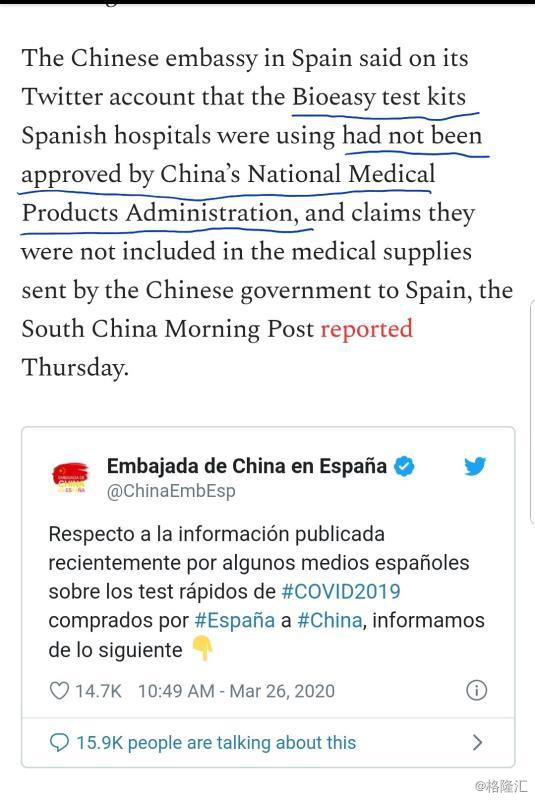 [size=+0]来源于:推特 [size=+0]来源于:官方文件 [size=+0]值得说明的是,虽然疫情期间,[size=+0]诊断试剂行业[size=+0]之中或存有一些鱼目混珠之象,但疫情的突发还是或将为[size=+0]诊断试剂行业[size=+0]中具备一定技术优势的企业带来机遇,根据[size=+0]相关券商给出的研报,相关以下个股或将可以关注: [size=+0]试剂盒概念的相关个股 [size=+0]迈克生物(300463.SZ)[size=+0]:[size=+0]公司[size=+0]属于医疗器械细分领域下的体外诊断行业,主营业务为体外诊断产品的研发、生产、销售和服务。2018年实现营业收入26.85亿元,同比增长36.31%,医疗器械服务行业已披露年报个股的平均营业收入增长率为25.90%;归属于上市公司股东的净利润4.45亿元,同比增长18.92%,医疗器械服务行业已披露年报个股的平均净利润增长率为34.14%;公司每股收益为0.80元。2019年营业总收入为32.23亿元,比上年同期增长20.02%;归属于上市公司股东的净利润为5.28亿元,比上年同期增长18.66%。[size=+0]此前[size=+0]公司收到国家药品监督管理局颁发的《医疗器械注册证》,[size=+0]其[size=+0]产品名称[size=+0]为[size=+0]新型冠状病毒2019-nCoV 核酸检测试剂盒(荧光 PCR 法)[size=+0]([size=+0]公司分子诊断平台下新产品[size=+0])[size=+0],有效期至2021年2月28日。 [size=+0]硕世生物(688399.SH)[size=+0]:[size=+0]公司是[size=+0]以分子诊断技术为核心,是集高端诊断试剂、仪器、第三方医学检验服务为一体的整体解决方案的国家高新技术企业[size=+0],[size=+0]于2019年12月5日在上海证券交易所科创板上市[size=+0]。2019年营业总收入为2.91亿元,比上年同期增长26.14%;归属于上市公司股东的净利润为8921.79万元,比上年同期增长39.79%。[size=+0]此前[size=+0]上海临床检验质量控制中心公布2020调查计划新型冠状病毒(2019-nCoV)核酸检测结果报告,泰州硕世医学检验实验室以“100%符合”成绩满分顺利通过[size=+0]。 [size=+0]华大基因(300676.SZ)[size=+0]:公司[size=+0]通过基因检测、质谱检测、生物信息分析等手段,为医疗机构、科研机构、企事业单位等提供基因组学类的检测和研究服务。2018年[size=+0]实现[size=+0]营收为25.36亿元,同比增长21.04%;净利润为3.87亿元,同比下降2.88%;2019年实现营业收入28.21亿元,同比增长11.22%;实现净利润3.01亿元,同比减少22.1%。[size=+0]此前公司[size=+0]宣布,[size=+0]其新型冠状病毒核酸检测试剂盒获得美国食药监局(FDA)紧急使用授权(EUA),是国内首个获得该授权的企业[size=+0],这是继该检测产品根据美国《新型冠状病毒肺炎在公共危机下的诊断检测政策指南》规定可面向美国临床市场进行商业销售之后,获得的正式进入美国临床市场销售的资质。截至目前,[size=+0]该公司[size=+0]累计生产该试剂盒700多万人份,已在全国完成近58万人份的新冠病毒核酸检测[size=+0],[size=+0]且相关[size=+0]订单已覆盖70个国家和地区。
|